氧化还原反应方程式的配平 1.掌握氧化还原反应方程式的配平原则和步骤,应重视新旧知识间的联系,即与以前所学氧化还原反应的基本概念以及与元素化合物间的反应密切结合。 2.掌握氧化还原反应方程式的配平方法,应注意记住一些典型的例子和反...

氧化还原方程式的配平方法有哪些
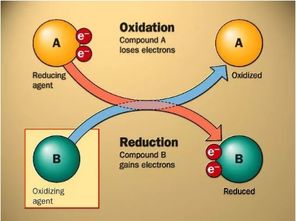
发生氧化还原反应时,还原剂失去电子、氧化剂得到电子。因为整个过程的本质好比是还原剂把电子给了氧化剂,在这一失一得之间,电子守恒。
万能的氧化还原反应配平方法
首先,明确氧化剂还原剂和它们对应的还原产物氧化产物。然后看氧化剂被还原成氧化产物得到了多少电子,还原剂被氧化成氧化产物又失去了多少电子,这样可以确定氧化剂和还原剂的物质的量之比,剩下的就简单了。
以高锰酸钾氧化氯离子为氯气的离子方程式为例:
1molMNO4-被还原生成MN2+,得到5MOL电子。1mol氯离子被氧化成氯气,失去1MOL电子,所以高锰酸根和氯离子物质的量之比是1比5,但是1MOL氯离子被氧化生成0.5MOL氯气,为了取整,所以同乘以2,得到MNO4-比CL-比CL2是2比10比5.
所以2MNO4- +10CL-(向右箭头)2MN2+ +5CL2
看左右两边,氧元素减少了,又因为是酸性条件,所以氧会和氢离子结合生成水。减少了8MOL氧原子,所以氢离子是16MOL,生成8MOL水。
所以最终的方程式是2MNO4- +16H+ +10CL-=2MN2+ +5CL2 +8H2O
氧化还原方程式配平的技巧
氧化还原反应的配平:
1.标出化合价并计算出价态的变化量;
2.使化合价的升降总数相等;
3.再观察非氧化还原部分中的金属的个数;
4.最后配平氢氧的个数
对于氧化还原反应可以采用电子守恒的办法
根据物质得到 的电子数,等于 失去的电子数
体验:五种配平方法解一题
配平方程式: Fe2O3+C——Fe+CO2
体验过程:
1、最小公倍数法:寻找化学反应方程式左右两边各出现一次的原子,且原子个数相差最多的元素为配平起点。
Fe2O3+C----Fe+CO2 选择O原子为配平起点,由于3与2的最小公倍数为6,故Fe2O3系数为2,而CO2的系数为3,然后调节C与Fe2O3的系数分别为3和4,既原方程变为:2Fe2O3+3C 高温 4Fe+3CO2
2、奇数配偶法: 寻找反应式左右两边出现次数较多的原子,且原子的个数为一奇一偶的元素为配平的起点。将奇数的原子用2、4、4、8….等偶数配成偶数,调节其他元素的原子的个数。
Fe2O3+C----Fe+CO2 选择O原子,因O原子的个数为一奇一偶,所以先将 Fe2O3用偶数2配平,再依次推导出C、Fe2O3 、CO2的系数,分别为3、4、3,即得2Fe2O3+3C 高温 4Fe+3CO2
3、观察法:当反应方程式两边有的物质组成较为复杂时,考虑用观察法。即观察分析反应式左右两边相关物质的组成,从中找出其变化规律来确定各自化学式前的系数;在推导其他原子的个数。
Fe2O3+C----Fe+CO2 反应中:C-----CO2 ,C夺取了Fe2O3 里两个O原子,那么一分子的Fe2O3 里的3个O原子可以供给3/2个C-----3/2个CO2,然后调节为整数系数为:2Fe2O3+3C 高温 4Fe+3CO2
4、电子得失法:配平方法:寻找反应式左右两边有一元素反应前后化合价降低或升高,即有一元素原子得到或失去电子,必有另一元素原子或电子,但化合价升降或降升总数相等,即电子得失总数相等,然后根据原子得失电子总数相等来确定其配平系数。
Fe2O3+C----Fe+CO2 反应中:
Fe2O3→Fe,Fe 的化合价由+3-----0价得3e×4
C →CO2,C的化合价由0价----+4价,失4e×3
3与4的最小公倍数为12,故得3 ×4与 4×3,方程的系数为2、3、4、3,即
失4e×3
+3 0 0 +4
2Fe2O3+3C 高温 4Fe+3CO2
得3e×2×2
5、待定系数法:化学反应的左右式子的各物质的分数系数均不知道,可以用不同的未知数代表式中各物质的化学式前的系数,然后依据质量守恒定律列出各种元素的原子相等的关系式,先令一个字母的数值进行求解,得出各字母的数值,最后代入原反应式中,即配平的化学反应方程式。
Fe2O3+C----Fe+CO2
设原方程式变为aFe2O3+bC----cFe+dCO2
因为 Fe:2a=c 令a=1则c=2 ;b=3/2; d=3/2
O:3a=2d
C:b=d
所以:2Fe2O3+3C 高温 4Fe+3CO2
实践1
配平 NH3 + O2—— NO + H2O
实践2
解出此方程式中的X、Y、Z及Q:XNaHCO3 YNa2CO3+ZCO2 +QH2O
实践题答案
实践1
指点迷津 是氧化还原反应,采用电子得失法配平。
NH3----NO N元素的化合价由-3 ---+2,失去5e
O2------NO O 元素的化合价由0-----2, 得到2e
O2------H2O O 元素的化合价由0-----2, 得到2e
失电子5,得电子为2+2=4,故得失总数为5×4=20,即NH3的系数为4,NO系数也为4,推出H2O的系数为6,而右边O原子为10个,既O2系数为5。
实践略解: 4NH3+5O2 4NO+6H2O
实践2
指点迷津 根据题目特征,用待定系数法可以很快解出。
实践略解: 因为 N: X=2Y 令 X=1,则Y=1/2 Q=1/2
H: X=2Q Z=1/2
C: X=Y+Z
O: 3X=3Y+2Z+Q
所以 原化学方程式变为NaHCO3= 1/2Na2CO3+1/2CO2 +1/2H2O
即2NaHCO3 = Na2CO3+CO2 +H2O
氧化还原反应的化学方程式配平有哪些方法
标签: 氧化还原方程式的配平 高中化学