热力学三大定律内容及公式目录
热力学三大定律内容及公式
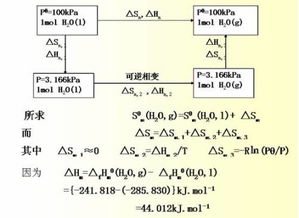
。
404 Not Found
。
。
。
。
。
。
。
。
高中物理热学公式
高中物理热学三大公式:
第一定律:内能的增量=吸收或放出的热量+物体对外界做的功或外界对物体做的功;第二定律:不可能使热量从低温的物体传递给高温的物体,而不引起其它变化;第三定律:热力学绝对零度不可达到。
一、热量计算公式
热量计算公式是热学中最基本的公式之一,其表达式为:Q=cmΔt其中,Q表示热量,c表物质的比热容,m表示物质的质量,Δt表示温度的变化。
这个公式说明,物体吸收或放出的热量与物质的比热容、物体的质量和温度变化有关。
从微观角度来看,热量是由于分子热运动加剧而产生的,因此物体吸收或放出的热量大小取决于物体的分子热运动的剧烈程度和物质的比热容。
二、热力学第一定律
热力学第一定律是能量守恒和转化定律在热现象中的表述,其表达式为:ΔU=Q+W其中,ΔU表示物体内部能量的变化,Q表示物体吸收的热量,W表示外界对物体所做的功。
这个公式说明,在热力学过程中,物体的内能变化等于物体吸收的热量和外界对物体所做的功之和。
三、热力学第二定律
热力学第二定律是描述热现象不可逆性的基本定律,其表达式为:不可能从单一热源吸收热量,并将其完全转化为功,而不引起其他变化。
这个定律说明,在热力学过程中,热量的转移和转化是有方向性的,不可逆转。
从微观角度来看,热力学第二定律是描述了自然界的自组织现象,即系统总是朝着熵增加的方向演化,最终达到熵的极大值状态。
综上所述,高中物理热学三大公式从不同的角度阐述了热现象的基本规律。
热量计算公式主要从宏观角度描述了物体吸收或放出的热量与物质的比热容、物体的质量和温度变化的关系。
热力学第一定律主要从能量守恒和转化的角度描述了物体内部能量转换和传递的过程;热力学第二定律主要从微观角度描述了热现象不可逆性的基本规律。
这些公式不仅为我们提供了解决实际问题的工具,更为我们揭示了自然界中深层次的规律和原理。
热力学定律

热力学第一定律W+Q=ΔU{(做功和热传递,这两种改变物体内能的方式,在效果上是等效的),
热力学第二定律 :不可能使热量由低温物体传递到高温物体,而不引起其它变化
第三定律:热力学零度不可达到
热力学的三个定律是什么?

热力学三大定律的本质
一、热力学第一定律的本质
在组成不变的封闭体系中,若发生了一个微小的可逆变化,则根据热力学第一定律,体系内能的变化为
dU = δQ + δW
由统计热力学原理可知,独立粒子体系的内能为U = ∑ni∈i,当封闭体系经历了一个可逆变化后,内能的变化为
(6-74)
上式右边的第一项∑∈idnI表示能级固定时,由于能级分布数发生改变所引起的内能变化值,第二项∑nid∈I则表示能级分布数固定时,由于能级改变所引起的内能增量。
从经典力学原理可知,对于组成不变的封闭体系,内能的改变只能是体系与环境之间通过热和功的交换来体现。
二、热力学第二定律的本质
由熵的热力学定义式及式(6-78),得
(6-79)
上式就是热力学第二定律的表达式,它表明可逆过程的熵变与能级分布数的改变有关。
而能级分布数的改变以为意味着体系的微观状态数发生了改变。
熵变是与体系微观状态数或热力学几率Ω的变化相联系的。
有公式:
S = kln Ω+ C (6-83)
式中C是积分常数。
若Ω=1时,S=0,则上式变成
S = klnΩ
此即Boltzmann定理的数学表达式。
由式可见,熵是体系微观状态数的一种量度。
微观状态数Ω较少的状态对应于较有序的状态,反之,Ω值大的状态对应于较无序的状态。
因此,微观状态数Ω的大小反映了体系有序程度的大小,亦即熵是体系有序程度或混乱程度的量度。
当Ω=1时,只有一个微观状态,体系最为有序,混乱程度为零,熵值为零。
基于以上讨论,我们可以作如下表述:在孤立体系中,自发变化的方向总是从较有序的状态向较无序的状态变化,即从微观状态数少的状态向微观状态数多的状态变化,从熵值小的状态向熵值大的状态变化,这就是热力学第二定律的本质。
三、热力学第三定律的本质
当T→0时,所有粒子都处于基态能级,此时Ω0=1,即把所有粒子放在一个能级上只有一个放法,体系只有一个微观状态,因此从玻兹曼定理,即式(6-25)可以得出结论:在0K时物质的熵值为零,即
S0 = klnΩ0 = kln1 = 0
上式可以看作是热力学第三定律的统计表达式,这与热力学第三定律的表述“在0K时任何纯物质的完美晶体的熵值为零”的结论是一致的。
标签:










